
EBI Décrypte : Le collagène
Le collagène, charpente invisible de notre organisme
Si la peau conserve sa fermeté, si les articulations amortissent les chocs et si les tissus résistent aux contraintes mécaniques, c’est en grande partie grâce au collagène. Cette protéine, la plus abondante de l’organisme animal, forme un véritable maillage de soutien qui assure cohésion, résistance et souplesse.
Les collagènes, une grande famille de protéines avec des fonctions multiples
Le corps humain comprend 28 types de collagènes, qui constituent les protéines majoritaires de la matrice extracellulaire. Ainsi, 30% des protéines de nos tissus sont des collagènes, toutes constituées de 3 chaines peptidiques qui s’organisent en triple hélice, sur une longueur variable. Au sein de cette région hélicoïdale, la glycine, le plus petit des acides aminés, est présente 1 fois sur 3, essentielle à la stabilité de la structure. Le remplacement de cette glycine par un acide aminé plus gros dans certains collagènes osseux peut être à l’origine de la maladie des os de verre.
Les collagènes présentent une grande diversité structurale leur permettant d’adopter des organisations variées et d’assurer des fonctions différentes. Ils peuvent ainsi former des fibres, des réseaux plans ou, pour certains, être insérés dans la membrane des cellules.
Les collagènes fibrillaires figurent parmi les plus abondants de l’organisme. Ils confèrent aux tissus résistance mécanique et cohésion tissulaire. Parmi eux, les collagènes de type I, III et V sont présents, en proportion variable, dans la peau, la paroi des vaisseaux, les tendons et l’os. Le collagène de type II est celui des cartilages, où il s’associe au collagène de type IX pour former des fibres. Un autre collagène important est le collagène de type IV. Il s’organise en réseaux plans et constitue le cœur de la structure qui permet à l’épiderme de s’ancrer fermement au derme dans la peau, la jonction-dermo-épidermique.
Ainsi, dans la peau, plusieurs types de collagènes sont présents dans le derme, l’hypoderme et à l’interface entre le derme et l’épiderme. Ils contribuent ainsi à la résistance mécanique de ce tissu en interagissant étroitement avec les cellules, mais aussi avec d’autres macromolécules comme l’élastine, composant majeur des fibres élastiques.
Une fabrication cellulaire très contrôlée
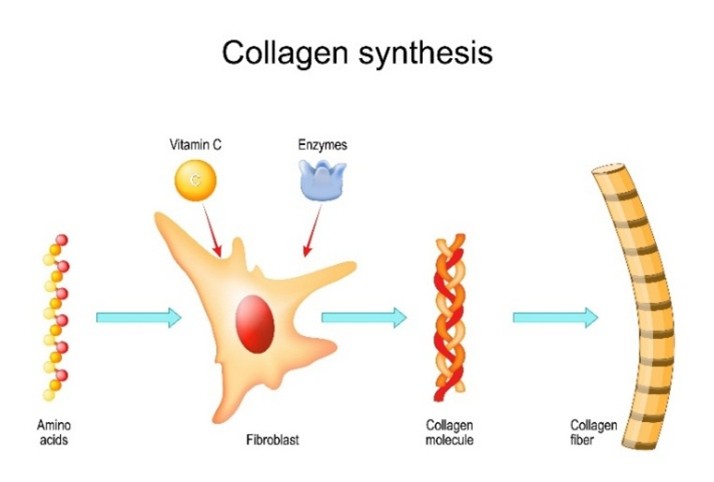
La production des collagènes fibrillaires est assurée par les fibroblastes, cellules architectes du derme. Ces collagènes, riches en acides aminés spécifiques comme la glycine, la proline et l’hydroxyproline nécessitent pour leur synthèse des cofacteurs essentiels, notamment la vitamine C et le fer. Une carence en vitamine C provoque le scorbut, pathologie bien connue des marins lors des longs voyages aux XVIème, XVIIème et XIXème siècle, caractérisée par une fragilisation des tissus.
Les fibroblastes synthétisent une forme précurseur, le procollagène, qui sera ensuite transformée et assemblée à l’extérieur de la cellule pour donner naissance aux fibres de collagène fonctionnelles.
Ce mécanisme est finement régulé. Par exemple, le début de la cicatrisation débute par une forte synthèse de collagène de type III, permettant une réparation rapide des tissus. Puis, progressivement, la synthèse de collagène de type I augmente, formant des fibres de plus en plus grosses pour renforcer la résistance mécanique du tissu cicatriciel.
Les facteurs de dégradation, ennemis silencieux des collagènes ?
Si la peau perd progressivement en fermeté et en élasticité avec l’âge, c’est en grande partie à cause de l’altération du collagène, dont le réseau se fragilise avec le temps : la peau perd en fermeté et les rides apparaissent.
Le premier facteur en cause est le vieillissement intrinsèque, aussi appelé vieillissement chronologique. C’est un processus naturel programmé par notre génétique. À partir de 25–30 ans, l’activité des fibroblastes — les cellules responsables de la production du collagène — diminue progressivement. La synthèse ralentit, tandis que les mécanismes de dégradation prennent le dessus. Le derme s’amincit, les fibres deviennent moins organisées et la peau perd progressivement en densité. Ce phénomène est inévitable, mais il reste lent et progressif lorsqu’il n’est pas aggravé par des facteurs extérieurs.
À ce phénomène naturel s’ajoute l’impact des agressions environnementales. Les rayons UV sont les principaux responsables du photo-vieillissement : ils génèrent des radicaux libres qui déclenchent un stress oxydatif qui active des enzymes appelées métalloprotéinases (MMP), chargées de fragmenter les fibres de collagène. A long terme, cela conduit à une désorganisation de la matrice dermique et à un phénomène appelé élastose solaire, caractérisé par une accumulation de fibres anormales et une perte de fermeté. Le tabac et la pollution accentuent également cette dégradation en augmentant la production de radicaux libres et en limitant la synthèse de nouvelles fibres.
Collagènes et produits du commerce
Les collagènes utilisés dans l’industrie (produits cosmétiques, compléments alimentaires) proviennent aujourd’hui majoritairement de sources animales (peau, os et tendons de bovins, peau, arêtes et écailles de poissons, sous-produits de l’aquaculture et de la transformation des produits de la mer). Le collagène d’origine marine est souvent mis en avant pour sa biodisponibilité. Il n’existe pas de collagène végétal à proprement parler. Les alternatives d’origine végétale (protéines de légumineuses ou polysaccharides) reproduisent certaines propriétés fonctionnelles du collagène (effet filmogène, hydratation), ou stimulent la synthèse endogène, mais ne remplacent pas la protéine dans sa structure biologique.
Les procédés d’extraction du collagène reposent sur plusieurs étapes successives visant à isoler et purifier la protéine tout en préservant sa structure. Après un prétraitement mécanique (nettoyage, découpe, broyage), les matières premières subissent un traitement chimique pour rompre les liaisons intermoléculaires et solubiliser le collagène. Une phase de purification est ensuite réalisée, suivie éventuellement d’une hydrolyse contrôlée pour produire des peptides à plus faible masse moléculaire. Aujourd’hui, les enjeux environnementaux et éthiques conduisent l’industrie à privilégier la valorisation des coproduits agroalimentaires, à réduire l’utilisation de solvants chimiques, à optimiser la consommation d’eau et d’énergie, et à renforcer la traçabilité ainsi que la durabilité des filières d’approvisionnement.
Collagènes à boire : que deviennent-ils vraiment dans l’organisme ?
Sous sa forme native, la molécule de collagène est trop volumineuse pour traverser la barrière intestinale. Elle doit être fragmentée en peptides plus petits pour être absorbée. Les recherches convergent vers une fenêtre optimale d’absorption située entre 500 et 3 000 Da. Dans cette plage, certains peptides sont absorbés quasi intégralement et ont été détectés dans le plasma sanguin dès 60 minutes après ingestion. Ces fragments passent ensuite dans la circulation sanguine. En revanche, ils sont redistribués selon les besoins de l’organisme et non exclusivement vers la peau. La biodisponibilité réelle, la dose efficace et la durée des effets restent des sujets de recherche actifs.
Vers des collagènes nouvelle génération
Pour répondre aux enjeux de sécurité sanitaire, de traçabilité et de durabilité, de nouvelles voies de production apparaissent, comme les collagènes recombinants produits par fermentation de micro-. Cette technologie ouvre des perspectives pour des ingrédients plus purs, reproductibles et indépendants des ressources animales.
L’approche EBI : du laboratoire au marché
Comprendre les collagènes, c’est croiser la biologie cellulaire, la physico-chimie des protéines, la physiologie cutanée, mais aussi les questions de formulation, de biodisponibilité et d’allégations. Cette approche globale illustre pleinement les compétences développées à l’EBI. De l’analyse des mécanismes biologiques à l’évaluation de l’efficacité des ingrédients, les formations et projets menés à l’EBI permettent aux futurs ingénieurs d’acquérir une lecture scientifique des tendances du marché.
En écho à ce sujet, les étudiants de la Majeure Conception & Développement ont organisé, le 22 janvier, un séminaire scientifique consacré aux collagènes, qu’ils ont conçu de A à Z, avec des conférences‑expertises et des ateliers pratiques.
- Les pathologies héréditaires du tissu conjonctif – Karim SENNI (EBI)
- Collagènes et intégrité cutanée – Valérie HAYDONT (L’Oréal)
- Collagènes et compléments alimentaires – Mathieu BOUARFA (Nutrastream)
- Ateliers pratiques création de gummies et formulation de masques (Etudiants).
Un évènement à l’image de l’EBI : thématique scientifique au cœur de nos secteurs, organisation portée par les étudiants, approche mêlant rigueur scientifique, application concrète et esprit d’équipe.
Les étudiants de la Majeure Conception & Développement, Marjorie Lassalle, Karim Senni











